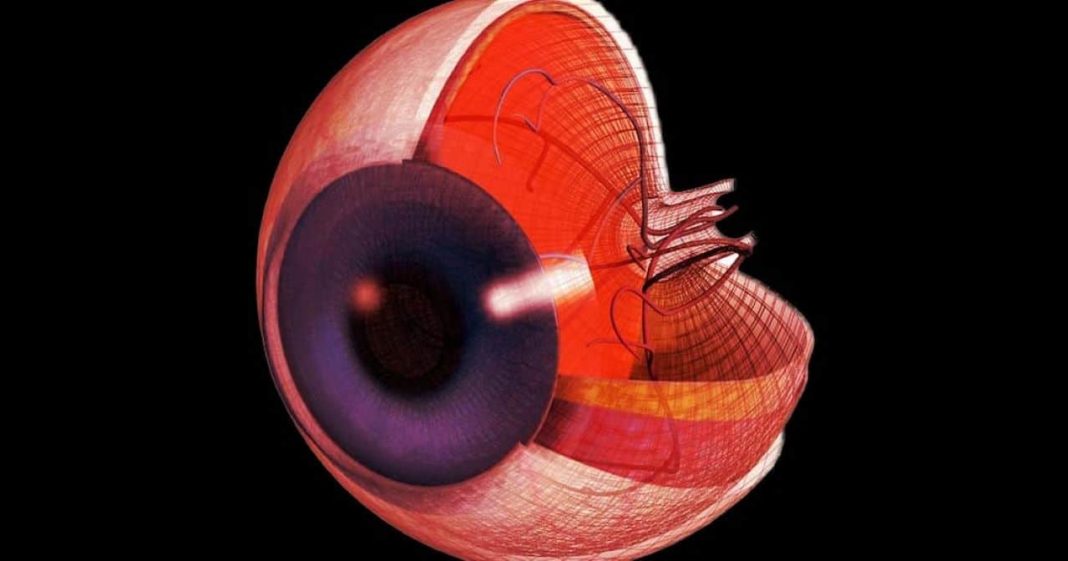
Os esforços de pesquisa sobre doenças do olho humano e funcionamento neural são prejudicados pelo fato de que esses órgãos se degradam rapidamente após a morte. Além disso, os olhos dos animais ainda são diferentes dos nossos. Para remediar isso, uma equipe internacional de pesquisadores desenvolveu um novo método para “trazer de volta à vida” retinas retiradas de doadores, 5 horas após sua morte. Este feito técnico permitirá novos estudos sobre o funcionamento do olho humano, do sistema nervoso, mas também sobre o prolongamento da vida útil dos órgãos a transplantar . Esse sucesso também oferece novas perspectivas para o tratamento de doenças neurodegenerativas, incluindo a degeneração macular relacionada à idade.
A morte é definida como a parada irreversível da atividade circulatória, respiratória ou cerebral. Muitos órgãos humanos periféricos podem ser transplantados de doadores falecidos usando protocolos para otimizar a viabilidade. No entanto, tecidos do sistema nervoso central e alguns órgãos associados, como os olhos, perdem rapidamente sua viabilidade após a interrupção da circulação, dificultando seu potencial para transplante. De fato, bilhões de neurônios no sistema nervoso central transmitem informações sensoriais na forma de sinais elétricos; no olho, neurônios especializados chamados fotorreceptores detectam a luz. Essas células morrem rapidamente depois que o coração para. No entanto, o curso do tempo e os mecanismos que causam a morte neuronal,
Para entender melhor como as células nervosas sucumbem à falta de oxigênio induzida pela cessação da atividade circulatória geral, uma equipe de pesquisadores americanos e suíços usou a retina como modelo do sistema nervoso central. Eles mediram a atividade de células murinas (ratos) e da retina humana logo após a morte e desenvolveram novos métodos para trazê-las de volta à vida. Seu trabalho é publicado na revista Nature .
Restaurando a comunicação celular após a morte
Para atingir seu objetivo, a professora associada de pesquisa da Scripps, Anne Hanneken, conseguiu fornecer mais de 40 olhos de doadores de órgãos, dentro de 20 minutos após a morte. Enquanto isso, Frans Vinberg, do Moran Eye Center, projetou uma unidade de transporte especial para restaurar a oxigenação e outros nutrientes aos olhos do doador, bem como um dispositivo para estimular a retina e medir a atividade elétrica de suas células. A equipe, portanto, procedeu em duas etapas.
Primeiro, os pesquisadores demonstraram o rápido declínio da sinalização neuronal e identificaram as condições necessárias para a potencial ressuscitação das células oculares in vivo em camundongos, após a morte e na retina humana. Em segundo lugar, eles mediram as respostas induzidas pela luz nos fotorreceptores maculares humanos dos olhos, retirados dos doadores, até 5 horas após sua morte. Eles foram então capazes de identificar os fatores modificáveis que levam à perda reversível e irreversível da sinalização luminosa após a morte.
Enquanto os primeiros experimentos reviveram os fotorreceptores, as células pareciam ter perdido sua capacidade de se comunicar com outras células na retina. A equipe identificou a privação de oxigênio como o fator crítico que leva a essa perda de comunicação.
Fátima Abbas, do Moran Eye Center e principal autora do estudo, explica em um comunicado à imprensa : ” Conseguimos despertar células fotorreceptoras na mácula humana, que é a parte da retina responsável por nossa visão central e nossa capacidade de ver detalhes finos e cores. Em olhos obtidos até cinco horas após a morte de um doador de órgãos, essas células responderam à luz brilhante, luzes coloridas e até mesmo flashes de luz muito fracos ”.
Usando sua abordagem inovadora para manter as células oxigenadas por longos períodos de tempo – prolongando o tempo que a retina e as células neuronais podem sobreviver – a equipe conseguiu restaurar um sinal elétrico específico visto em olhos vivos, “a onda b”. Este último atesta uma comunicação entre todas as camadas de células maculares que nos permitem ver. Esta é a primeira gravação post-mortem da onda b , feita a partir do centro de uma retina humana. No entanto, esse retorno temporário da atividade das células da retina não significa que os globos oculares do doador possam “ver”. Centros visuais superiores no cérebro são necessários para reviver todo o processo de visão.
Frans Vinberg diz: “ Conseguimos fazer as células da retina se comunicarem, como fazem no olho vivo para mediar a visão humana. Estudos anteriores restauraram uma atividade elétrica muito limitada aos olhos de doadores de órgãos, mas isso nunca foi alcançado na mácula, e nunca na extensão que demonstramos agora ”.
Diante desses resultados, alguns especialistas questionam a natureza irreversível da morte no sistema nervoso central. De fato, se é possível preservar certos órgãos do corpo humano para um transplante, o sistema nervoso central deixa de funcionar muito rápido para ser “recuperado”, na perspectiva de um transplante. No entanto, todos os elementos constituintes do nosso sistema nervoso não morrem na mesma velocidade, mecanismos de “sobrevivência” às vezes são estabelecidos por algum tempo, o conceito de morte é então mais complexo. Nesse contexto, os feitos descritos no artigo permitiriam ver as coisas com mais clareza (sem trocadilhos) e indicar novas possibilidades em termos de avanços médicos.
Estudar doenças neurodegenerativas
O processo demonstrado pela equipe poderia, portanto, ser usado para estudar outros tecidos neuronais do sistema nervoso central. Isso ajudaria os pesquisadores a entender melhor as doenças neurodegenerativas, incluindo doenças da retina que causam cegueira, como a degeneração macular relacionada à idade.
Além disso, potenciais terapias poderão ser testadas em células oculares humanas funcionais, possibilitando acelerar o desenvolvimento de tratamentos, sem o uso de animais de laboratório. De fato, Frans Vinberg ressalta que essa abordagem pode reduzir os custos de pesquisa em comparação com o trabalho em primatas não humanos e a dependência de modelos animais, produzindo resultados que nem sempre se aplicam a humanos. Por exemplo, embora os ratos sejam comumente usados na pesquisa da visão, eles não têm mácula, ao contrário de nós.
Além disso, Ann Hanneken diz que essas descobertas certamente ajudarão a produzir manchas viáveis de tecido da retina humana para tratar doenças que causam cegueira. Ela explica: “ Até agora, não foi possível fazer com que as células de todas as diferentes camadas da retina central se comunicassem como normalmente fazem em uma retina viva. No futuro, podemos usar essa abordagem para desenvolver tratamentos destinados a melhorar a visão e a sinalização luminosa em olhos com doenças maculares, como a degeneração macular relacionada à idade ”.
Por fim, este estudo agrega um corpus científico sobre a natureza irreversível ou não da morte. Em 2018, pesquisadores da Universidade de Yale conseguiram “reviver” o cérebro de um porco, 4 horas após sua morte, sem, no entanto, conseguir restaurar a atividade neuronal geral. O procedimento seguiu o mesmo esquema operacional, ou seja, a restauração da circulação sanguínea, permitindo o fornecimento de oxigênio e nutrientes essenciais. Os dados coletados por Abbas et al. poderia fornecer chaves valiosas para a compreensão de futuros experimentos post-mortem .
Fonte: Nature